結晶構造(Crystal structure)
多くの固体物質は結晶であり、原子レベルで見れば規則正しく原子が整列したパターンを持っています.これを結晶構造と呼びます.結晶構造を構成する最も小さな構成ユニットが単位格子(単位胞)であり、物質の「顔」とも言える非常に重要な情報です.
物質はそれぞれ異なっても、結晶構造を見ると同じもの、あるいはよく似たものが見つかります.科学者はこれらの共通するものをグループ化することで、共通する性質を比較したり類似の物質を合成する足がかりにしたりしてきました.
結晶構造には、その代表的な物質名や鉱物名から名前がつけられます.例えば、塩化ナトリウム型構造やペロブスカイト型構造は固体化学を代表する非常に有名な結晶構造です.新しい物質が発見されるにしたがって新しい結晶構造は増えていきますが、多くの物質は代表的な結晶構造に属します.
今回は、そのような代表的な結晶構造を紹介します.
単体の結晶構造
周期表には多くの元素があり、それぞれ性質が異なります.常温で金属のものから絶縁体、半導体まで様々な性質を示します.常温で固体のものもあれば、液体や気体のものもありますが、まあ極低温まで冷やせばどれも固体になるでしょう.
単一の元素からなる固体のうち、12族以下の金属元素は3種類の結晶構造のどれかに属します.すなわち、体心立方構造、面心立方構造、六方最密構造です.金属元素は全方向に等方的な化学結合(金属結合)を形成するため、できるだけ多くの原子が周りにいてくれた方が有利なのです.
これら基本的な3種類の結晶構造については以下の記事で解説しています.
一方、13族から17族のいわゆるpブロック元素ではまた異なる結晶構造が現れます.これらの元素は金属結合ではなく共有結合によって化学結合するため、一つの原子が結合する原子の数が限られ(例えば14族のシリコンでは4つの結合しかできない)、最密充填構造をとりません.*1
そして、同じ元素であっても異なる結晶構造をとる場合もあります.同素体です.炭素がダイヤモンド構造と黒鉛構造の両方をとりうることは有名でしょう.
化合物の結晶構造
化合物とはすなわち複数の元素を含む多元系の物質です.二元系、三元系から無限に多い系まで考えられますが、結晶構造として名前がつけられているのはせいぜい五元系ぐらいまでかなと思います(元素数が多すぎると物質の数も限られてくるので).
二元系の結晶構造
最も単純な組成はのように1:1の組成比を持つ物質でしょう.塩化ナトリウム型構造や閃亜鉛鉱型構造など、非常に有名な結晶構造が属します.
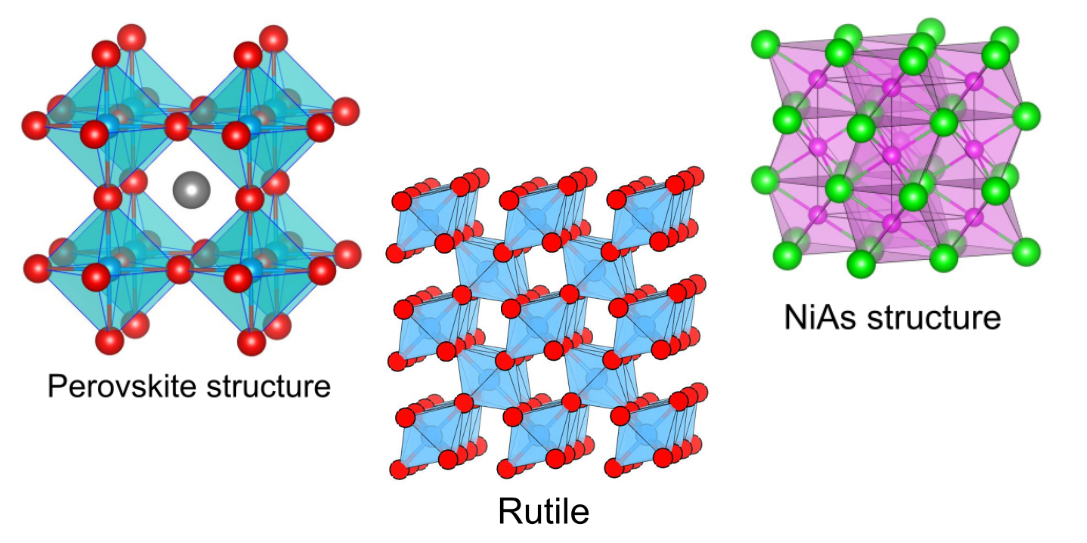
1:1の組成比を持つ結晶構造として代表的な塩化ナトリウム型構造、ヒ化ニッケル型構造、塩化セシウム型構造、閃亜鉛鉱型構造、ウルツ鉱型構造を解説しています.
1:1の組成比以外にも、1:2の組成比を持つ蛍石型構造、ルチル構造、パイライト構造、マーカサイト構造、ラーベス相、2:3の組成比を持つコランダム構造を解説しています.
三元系の結晶構造
三元系になると原子の並びのパターンはさらに複雑性を増し、より多様な結晶構造が現れます.中でも有名なのはペロブスカイト構造でしょう.太陽電池の名前のほか、誘電材料やイオン伝導体としてあらゆる分野で姿を見かけます.
ペロブスカイトに関連した結晶構造だけでもかなりの種類が知られます.
他にも三元系の結晶構造はあります.メジャーどころからマイナー寄りまで、スピネル構造、パイロクロア構造、ホイスラー合金、ThCr2Si2型構造、CaAl2Si2型構造の解説を行っています.
まとめ
ここで紹介したもの以外にも膨大な結晶構造が報告されています.あまり馴染みがなくても、眺めているだけでも面白いものです.ぜひともお気に入りの結晶構造を見つけてみてください.
参考文献
リンク先に記載
結晶構造の描画にはVESTAを使用.K. Momma and F. Izumi, "VESTA 3 for three-dimensional visualization of crystal, volumetric and morphology data," J. Appl. Crystallogr., 44, 1272-1276 (2011).
*1:例外はあり、pブロック元素でも最密構造をとるものもあります.