エレクトライド(電子化物、Electride)
物質中の価電子は原子と原子の結合に役割を果たし、概して原子の近くに存在します.非共有電子対(孤立電子対)は結合に関与しないことが多いですが、特定の原子の近くにあることには変わりません.いつでも原子と一緒にいた電子.そんな電子が物質中で原子から離れて存在することはあるのでしょうか.
電子が原子から離れて存在している物質、それがエレクトライド(電子化物)です.エレクトライドでは、電子は原子のいないサイトを単独で占め、あたかも負の電荷を持つ陰イオンであるかのように振る舞います.
エレクトライド中の電子は原子に束縛されていないため比較的自由に運動し、高い伝導性を誇ります.また、容易に物質外に取り出すことが可能なため、仕事関数が小さくなります.これらの特長により電子放出素子や電池材料、合成触媒、超伝導など様々な分野への展開が見られています.
原子から離れて一丁前に陰イオンのように振る舞う電子.今回は、そんな電子を含む不思議な物質、エレクトライドについて見ていきます.

エレクトライドとその発見
有機エレクトライドの発見
イオン結晶中で陰イオンが欠損し、代わりにそのサイトに電子が捕捉される場合があります.これは中心と呼ばれ、固体中に電子が単独で存在する例です.
ただし、中心における電子濃度は非常に低く、対してエレクトライドは非常に高い電子濃度を持ちます.それゆえ、
中心を持つ物質とエレクトライドとでは大きく異なる性質を示します.
エレクトライドの歴史は100年以上前に遡ります.舞台は溶液中のアンモニアです.アルカリ金属をアンモニア液中に溶解させた際、非常に濃い蒼色を呈することが発見されました.この着色の原因は、電子がアンモニアに溶媒和されたことに由来するとKrausが提案しました.この溶液中の電子は還元性に優れ、Birch還元の試薬として利用されます.
次いで1980年頃、James Dyeはエレクトライドに関する先駆的な研究を行っています.彼は、電子を捕捉する物質としてアンモニアに代わって有機分子を用いました.その分子はクラウンエーテルと呼ばれ、カゴ上の空間に金属イオンなどを取り込むことが可能な巨大分子です.

1982年、Dyeはクラウンエーテルと金属を組み合わせ、分子からなるカゴの中に電子を単独で捕捉することに成功しました.このように孤立した電子を持つ物質はエレクトライドと呼ばれるようになり、さらにアルカリ金属と組み合わせることでアルカリ金属陰イオン(アルカライド)の合成にも成功しています.
しかし、分析技術が限られていた当時、本当に物質内の空間に電子が存在するかどうかを確かめることは困難でした.Singhらは理論計算手法を発達させ、電子密度がの周りではなく孤立した空間中に存在することを示し、エレクトライドの存在を裏付けました.
エレクトライドが存在することが明かされ、研究も加速しました.しかし、問題もあります.クラウンエーテルによって生成した「有機エレクトライド」は非常に不安定だったのです.空気や湿気で容易に分解するどころか、氷点下でしか存在が許されませんでした.
有機エレクトライドから無機エレクトライドへ
安定なエレクトライドは、思いもよらない物質で実現しました.マイエナイト()という複雑な物質は、セメントの材料として知られています.この材料は、
からなる正電荷を持つカゴを構造中に持ち、カゴの一部には酸素イオンが含まれます.
を還元するとカゴ中の酸素イオンが電子と入れ替わり、なんとエレクトライドが生成しました.

この「無機エレクトライド」は例外的に非常に安定で、空気中に放置しても手で触っても問題ありません.安定なエレクトライドが得られたことで研究が促進され、エレクトライドの興味深い電子物性が知られるようになりました.
例えば、は常温で安定にも関わらずアルカリ金属並みに電子を取り去りやすい性質があり、様々な化学反応に寄与します.また、極低温で超伝導を示すことも明らかになりました.
様々なエレクトライド
では電子はカゴの中に閉じ込められています.すなわち、電子が孤立したゼロ次元のエレクトライドと区分することができます(ただし、電子はカゴの間を移動する事ができます).物質開発が進み、別の次元性を持つエレクトライドも発見されました.
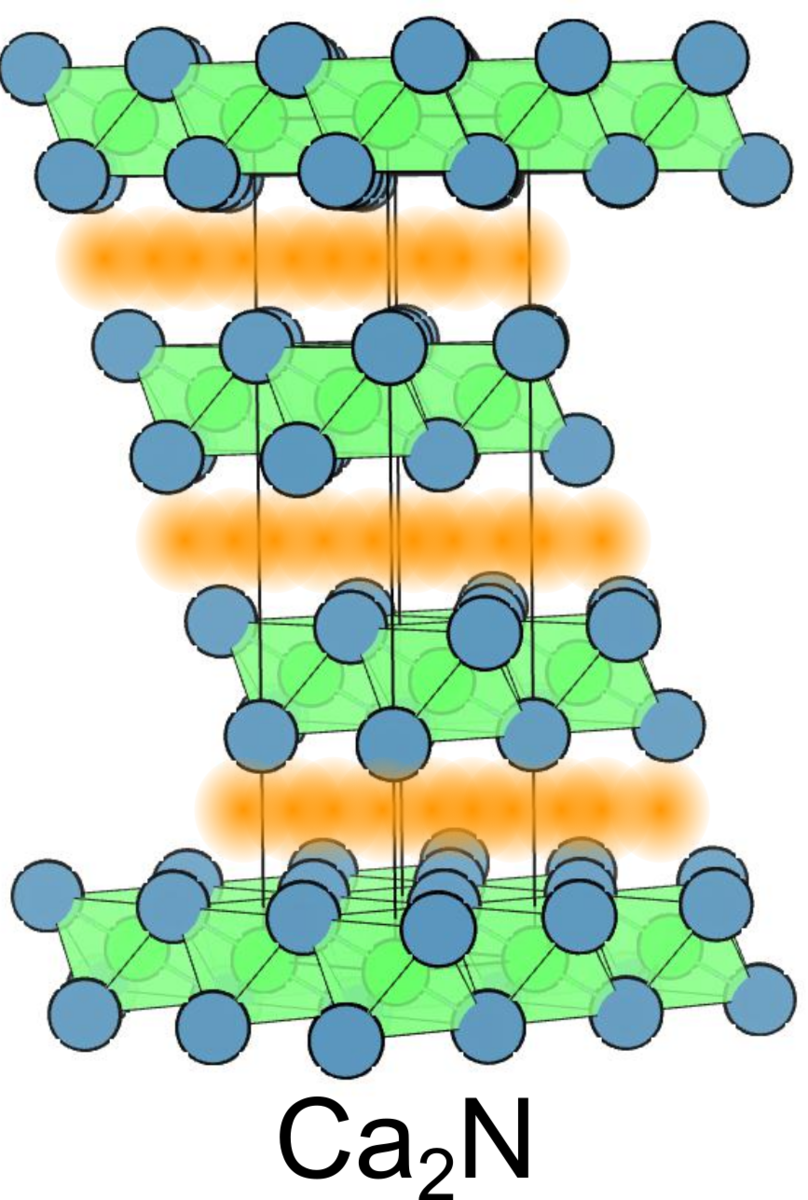
は層状構造をもち、正の電荷を持つ層の間に電子が位置しています.すなわち、二次元的なエレクトライドと言えます.
における電子の移動度は非常に高く、低温ではさらに増強されます.同様の結晶構造を持つ
や
なども二次元エレクトライドであることが報告されています.
その後、や
のような一次元エレクトライド、高圧でのみ姿を見せる高圧エレクトライド、結晶構造を持たないアモルファスエレクトライド、トポロジカル材料に概念が拡張されたトポロジカルエレクトライドなど、様々な特徴を持つエレクトライドが続々と発見され、それぞれ特有の興味深い性質を示します.
エレクトライドの機能
いくら珍しい物質であっても、役に立たなければ「興味深い」で終わってしまいます.しかし、エレクトライドは工業的にも利用価値のあるような様々な性質を示すことが見出されています.
電子を放出しやすい性質
物質から一つの電子を引き剥がすために必要な最小エネルギーを仕事関数と呼びます.陽イオンになりやすいアルカリ金属などは仕事関数が小さく、安定な貴ガス元素の仕事関数は大きな値です.
孤立した電子を持つエレクトライドは特に小さな仕事関数を示します.これは安定な無機エレクトライドにおいても例外ではなく、の仕事関数はアルカリ金属に匹敵します.安定なのに電子を取り出しやすいという一見矛盾した特性を活かし、触媒材料などにむけた材料開発がされています.
優れた電子伝導性と超伝導
エレクトライドは、その次元性によって電子特性が顕著に変わります.は高い電子伝導性を示す二次元エレクトライドですが、高圧下では構造相転移によって1次元(または0次元)になり、それに伴って金属から半導体へと変貌します.
また、前述の通りは低温で超伝導を示します.すなわち、孤立したエレクトライド中の電子でも超伝導を起こすのです.また、
などでも低温で超伝導が確認されています.
磁性
電子は電荷の他に磁石としての性質も示します.物質中で孤立した電子がどのような磁気特性を示すかは興味深いところです.は電子それぞれが孤立しており、目立った磁気物性を示しませんが、物質によってはエレクトライドであっても特筆すべき磁気物性を示します.
は強磁性体(磁石)であることが理論的に予測され、実際に強磁性を示すことが実証されました.
自体も磁気モーメントを持ちますが、
において観測される磁気モーメントは
だけを考慮に入れた値よりも大きく、孤立した電子が磁気モーメントを持っていると解されています.他にも、
などで強磁性状態が見出されています.
触媒特性
電子を与えやすいが安定な物質は、「反応を促進するが自身は変換されない物質」として触媒材料への適用が考えられます.遷移金属ナノ粒子をエレクトライドの表面に固定した場合、電子がエレクトライドから遷移金属に移動し、遷移金属表面に吸着した様々な分子を活性化させる事が可能です.
これにより、堅固な窒素分子の三重結合でさえも乖離し、窒素分子と水素分子からアンモニア分子を生成するための触媒材料として機能します.アンモニア合成反応は20世紀初頭にハーバー・ボッシュ法が確立されて以来同じ鉄系触媒材料が使用されていますが、エレクトライドはこれを置き換える可能性があるとして注目されています.
また、アンモニア合成反応以外にもアンモニア分解反応、還元剤、クロスカップリングなど種々の有機反応へと展開されています.
エレクトライド物質
C12A7
アルミナセメントの主成分であり、典型的な絶縁体として知られていました.正の電荷を持つカゴ型物質であり、カゴの中に酸素イオンが含まれます.この酸素イオンを電子に入れ替えたエレクトライドは非常に安定であるにもかかわらず低い仕事関数の値を示します.
カゴの中の酸素イオンは別の陰イオン種にも置換可能で、水素陰イオンや酸素分子イオン、果ては金の陰イオンなどが含まれる材料も合成可能です.
二次元エレクトライド
は、電子が層内に閉じ込められた二次元エレクトライドであり、層間の方向に比べて層方向に極めて高い電気伝導度を示します.
と同様の構造を持つエレクトライドが理論的に予測され、
や
、
などが発見されました.
系と異なり、これらの二次元エレクトライドは空気や湿気によって容易に分解します.
一次元エレクトライド
や
は一直線に連なった一次元的な結晶構造を持つ物質群であり、一次元エレクトライドとして知られます.二次元エレクトライドとは異なり、空気や水では分解しません.
はエレクトライドとしては極めて珍しく、遷移金属である
を持ちます.通常、エレクトライドの電子は金属イオンを還元する能力が非常に強いので、遷移金属が含まれる系で現れることはレアでした.
金属エレクトライド
エレクトライドはイオン結合性の物質での例が主ですが、エレクトライドの概念は金属材料へも拡張が可能です.金属元素のみからなるにおいても、結晶構造中の隙間に電子が存在することが提案され、実際に結晶中の電子が水素と反応して水素陰イオンが生成することが示されました.他にも種々の金属間化合物のエレクトライドが発見されています.
まとめ
エレクトライドが生成するための条件は、結晶構造中に正の電荷を持つ隙間が存在することです.負の電荷を持つ電子はその隙間に入ることで安定化され、エレクトライドとなります.口で言うのは簡単ですが、そのような物質は必ずしも多くありません.型構造やペロブスカイト型構造のような基本的な結晶構造を考えれば、そのような不自然な隙間が存在すること自体が非自明であることに気づきます.
カゴ型の隙間が存在する物質は多くはないとはいえ、知られているものもあります.ゼオライトはケイ素とアルミニウムを含む酸化物で負に帯電したカゴ型の隙間を持ち、ここに水素イオンやアルカリ金属イオンが入ります.シリコンなどのネットワークをもつ無機クラスレートでは、カゴの中にアルカリ土類金属や希土類金属が入ります.ゼオライトとはカゴの帯電の符号が異なるため、正の電荷を持つカゴ状物質を「逆ゼオライト」と呼ぶ向きもあるとかないとか.
参考文献
Journal of Materials Chemistry C 8.31 (2020): 10551-10567.
Chemical Reviews 121.5 (2021): 3121-3185. およびこれらの総説中の各種文献
細野先生による詳細な解説が多く利用できるので、そちらも参照のこと
結晶構造の描画にはVESTAを使用.K. Momma and F. Izumi, "VESTA 3 for three-dimensional visualization of crystal, volumetric and morphology data," J. Appl. Crystallogr., 44, 1272-1276 (2011).