金はなぜ金色か
金は、他の金属では再現できない独特の輝きを持ちます.古来より王侯貴族を魅了してやまない黄金色はどのようにして生まれるのでしょうか.
今回は、金が何故金色を示すのかという禅問答のような疑問を見ていきます.

周期表と金の性質
誰もが高校化学で周期表を習ったことがあると思いますが、授業で習うのは周期表の上の方にある元素に限られていたことでしょう.周期表の下の方にある元素(重元素)では、上の方にある元素(軽元素)とはまた異なる振る舞いが見られます.
周期表の下側に進めば原子半径は大きくなるとされていますが、重元素ではそうなるとは限りません.11族元素を見ると、では原子半径が増加しますが、
では原子半径はむしろ小さくなります.
金には他にも不思議な性質があり、電気陰性度が非常に大きいという特徴を持ちます.他にも、重元素である金属は酸化数にも決まった性質が現れます(後述).
重元素におけるこれらの特徴の起源として、以下の2つの要因が挙げられます.
(2)相対論効果
順番に見ていきましょう.
(1)ランタノイド収縮
(1)のランタノイド収縮は、その名の通りランタノイドに関係があります.ランタノイドは周期表の下部に分けて書かれることが多く、4f電子を持つという特徴があります.4f電子は電子の遮蔽が弱いことが知られており、この影響で原子半径を小さくする効果があります.
この現象(ランタノイド収縮)の影響で、ランタノイドの原子核を含んだ元素はいずれも原子半径が顕著に小さくなります.金や水銀といった重金属が、周期表で直上にある元素よりも原子半径が小さいのはランタノイド収縮が要因の一つとなっています.
(2)相対論的効果
(2)の相対論的効果は、アインシュタインの相対性理論による影響を考慮したものであり、これによって重金属の異常な性質の大部分を説明することができます.アインシュタインは、1905年に発表した特殊相対性理論において、運動する物体の質量がその速度に応じて増加することを提唱しました.(は光速)
この効果は、物質内の電子についても働きます.水素原子においては、電子の速度は高速の程度であるとされ、電子の相対論的質量は静止質量の1.00003倍とほぼ無視できます.しかし、金や水銀といった重金属においては無視できない値となります.
水素より重い原子における1s電子の平均的な半径方向の速度は、以下のように与えられます.
これは金の場合、となり、光の58%の速度を持つことになります.質量は静止質量の1.23倍となり、1s軌道は23%と大きく縮みます.同様に外側にある電子軌道も大きく縮むことになります.
相対論効果の影響を簡単にまとめると以下のようになります.
(1) s軌道とp軌道の収縮が大きい
(2) s軌道とp軌道が収縮した影響で、d軌道とf軌道が外側に拡張される
(3) 「スピン軌道相互作用」により各電子軌道のエネルギーが分裂するが、この効果は重い元素ほど大きい
色の違いとエネルギー図
これらの効果の合計は、重金属である金では非常に重要となります.
相対論効果に基づき、金がなぜ金色であるかを説明することが可能です.以下に、金と銀における電子軌道のエネルギーを示します.
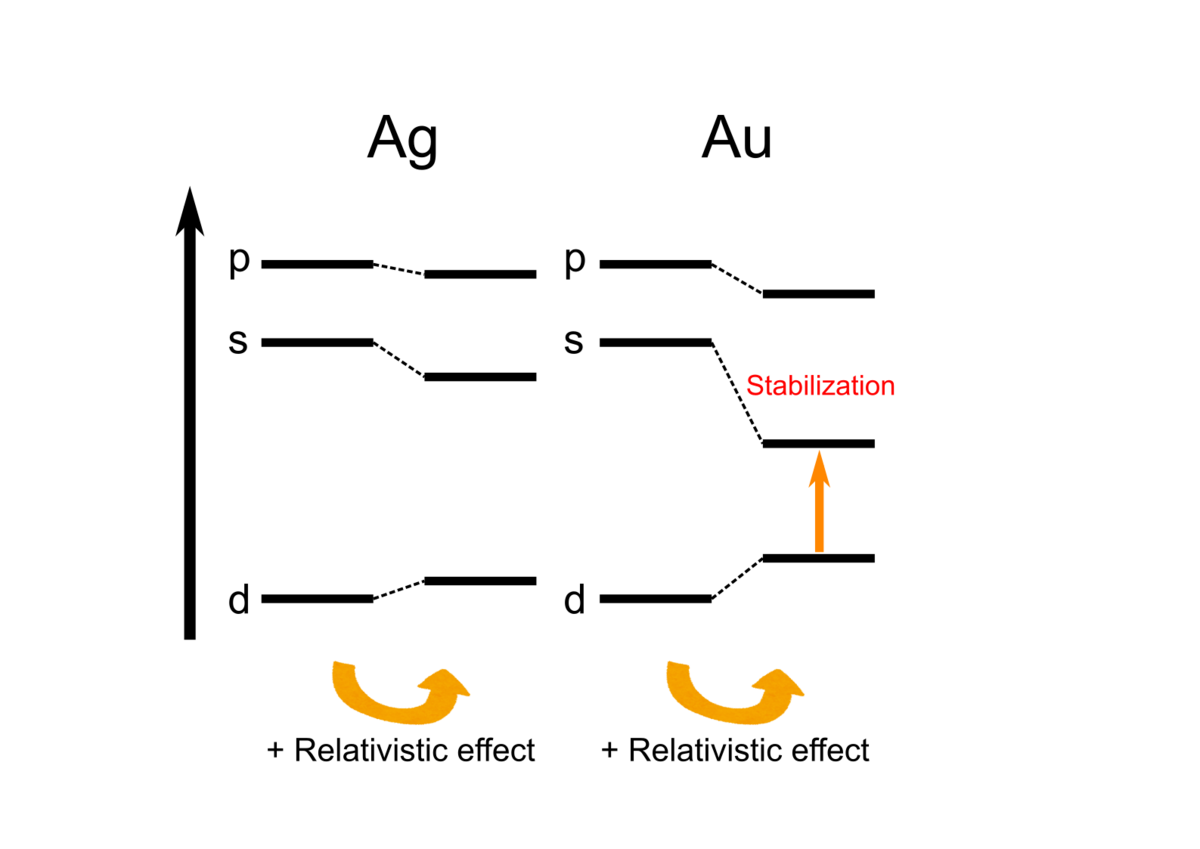
金では、相対論効果を考慮しなければ6s軌道と5d軌道はエネルギー的に遠くはなれています.ここで相対論効果を考慮すると、6s軌道のエネルギーが下がると同時に5d軌道のエネルギーが上がり、両者の差が一挙に縮まります.
このエネルギー差が小さくなったことで可視光を吸収できるようになり、金が黄色がかった色を示すようになります.一方、銀では相対論的効果が小さいため可視光を吸収することができません.
このエネルギー図から、金と銀のイオン化エネルギーの定性的な違いも説明することが可能です.金から1つ目の電子を放出させるイオン化エネルギーは、銀のものよりも少し大きい程度ですが、2つ目、3つ目となると銀のほうがはるかに大きいです.すなわち、は
よりも現れやすいですが、
は
よりも容易に生成します.
金の電気陰性度が大きいことについても説明がつきます.金における最もエネルギーの高い電子軌道は6s軌道であり、これは相対論効果によって安定化されています.安定化された軌道にもう一つ電子が入るスペースが有るのですから、電子を引きつける能力が高いのも納得です.
この影響により、気体状態において金分子は非常に生成しやすいことが知られています.また、金の高い電気陰性度を反映して、金が負の電荷を持つアニオンとして振る舞う物質も報告されています.
参考文献
Journal of Chemical Education 68.2 (1991): 110.