
更新 2024-3-3
物質と分類
X線回折測定やNMRの発展により物質のミクロな構造が分かるようになると、結晶構造や電子配置による物質の分類も進むようになりました.特に、価電子の数が物質の構造・性質を決める上で重要な役割を担うことが明らかにされ、価電子数は物質を分類する上で無視できないパラメータとなりました.
有名なオクテット則(8電子則)は物質の価電子数に基づいており、有機化学や典型元素からなる無機物質で見られる最も基本的なルールです.18電子則はオクテット則を遷移金属を含む有機金属錯体に拡張したものです.VSEPR則は錯体や分子の形状を予測することに威力を発揮し、Wade-Mingos則はホウ素などからなるクラスターの構造を決定し、Hume-Rothery則は合金が生成するためのルールを定めます.
物質が発見されればされるほど共通項を持つ物質が増えていき、そのたび物質を記述するルールも考案されていきます.ルールが分かれば、それに基づいて新しい物質を予測するためにも活用できます.
しかし、せっかく作ったルールでも破ってしまう物質があります.近年で最も重大なルール違反は準結晶の発見ですが、ルールが破られると科学者は新しいルールを制定します.ルールが破られるには何らかの事情があるはずで、事情を汲むことで物質への理解も深まります.
今回の主題であるジントル相(Zintl相)もまた、専用の新しいルールが制定された物質たちです.
Zintl相(Zintl phase)
元素ごとに電子を引きつける能力は異なり、この値は電気陰性度として定量化されます.元素と元素が化合物を形成するとき、元素の電気陰性度の違いによって結合の仕方が大きく異なることが知られています.例えば、電気陰性度の差が大きければ、イオン結合を形成します.
イオン結合性の物質では、電気的に陽性な元素から陰性な元素に電子が移り、前者はカチオン、後者はアニオンとなります.それぞれが閉殻構造(オクテット)を満たすイオンとなり、異符号のイオン同士のクーロン力によってイオン結合を形成します.電子は各イオンに束縛されており、それゆえイオン結合性の物質は一般的に絶縁体です.
化学結合には様々な種類のものが知られていますが、代表的なものはイオン結合、金属結合、共有結合です.これら3つの化学結合は、ケテラーの三角形に現れる結合として知られています.ケテラーの三角形とは、化合物の結合様式を、構成元素の電気陰性度を元に整理した図です.詳しくは、以前の記事で紹介しています.
ケテラーの三角形の頂点には、前述のイオン結合、金属結合、共有結合が位置するわけですが、三角形の内部に見慣れない領域が存在しています.イオン結合と金属結合に位置する領域に多くの化合物が生息しており、Zintl相と呼ばれます.
Zintl相の化合物は、ケテラーの三角形から予想されるとおり、イオン結合と金属結合の中間的な性質を示し、イオン結晶にも金属にも分類できません.半導体的な電気伝導を示し、融点が高く、セラミックス(酸化物絶縁体)のような脆さと金属的な光沢を併せ持ちます.
これらの物質は1930年頃、Edward Zintlによって詳しく研究され、後にZintl相と呼ばれる新しいクラスの化合物の電子構造と結合を合理的に説明する基礎が築かれました.KlemmがさらにZintl相の概念を発展させたため、Zintl相を記述するルールはZintl-Klemm則と呼ばれます.
Zintl相に属する物質
実際にZintl相に属する物質を見ていきましょう.は最初期に研究されたZintl相の一つです.結晶構造を見ると、
は孤立しており、
がダイヤモンド構造のように四配位のネットワークを形成しています.
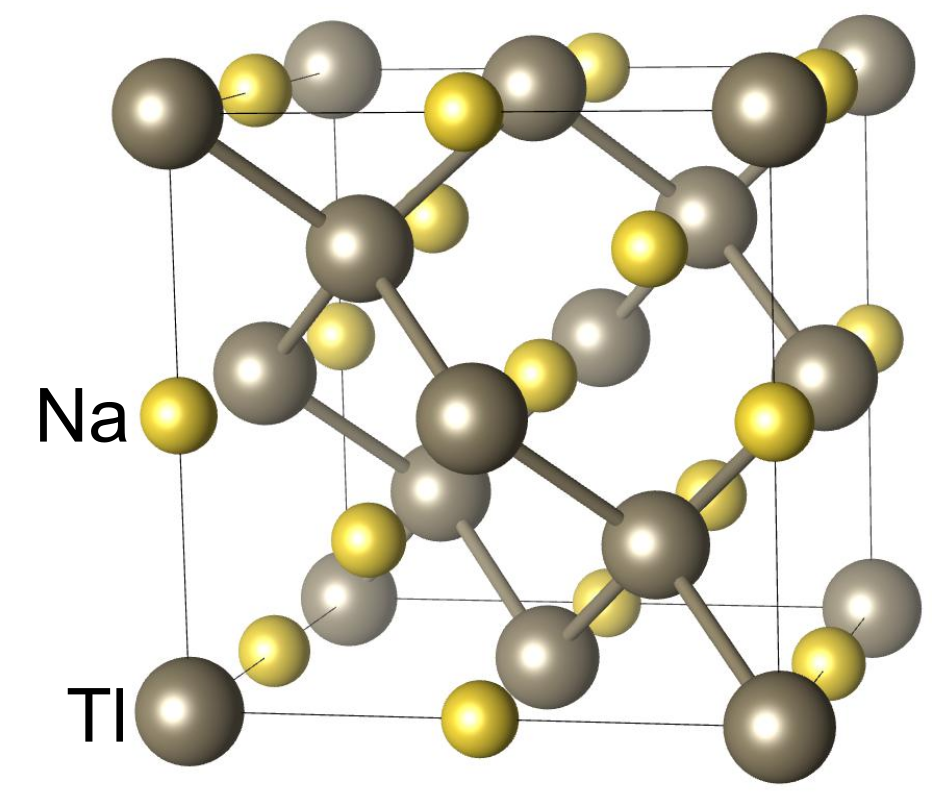
この電子状態を、Zintl-Klemm則では以下のように考えます.
と
では
の方が電気的に陽性です.そのため、
の電子は
に移り、1価の
イオンができます.イオン結合性の
と異なる点は、このままでは電子をもらった
がオクテット則を満たさないことです.
はオクテット則を満たすため、周囲の他の
と共有結合を形成します.
は13族元素であることから、電子を一つ受け取ると14族と同じ電子配置となります.14族元素は、ダイヤモンドやシリコンの結晶構造を思い浮かべてみれば分かるように、原子一つあたり4本の共有結合を形成します.
それゆえ14族元素と同じ電子配置を持つは、
や
ように四配位のダイヤモンド状ネットワークを作るわけです.
Zintl相の特徴
このように、Zintl相では負の電荷を受け取った典型元素がオクテット則を満たすように共有結合を組みます.一般的には、陽イオンとしてアルカリ金属およびアルカリ土類、陰イオンとして13族、14族、15族元素を含むような物質がZintl相とされます.
まとめると、Zintl化合物とは以下のような規則を満たすような物質群です.
- アルカリ金属またはアルカリ土類金属、およびpブロックの元素からなる
- 電気的に陽性な元素から陰性な元素に価電子を渡し、後者はオクテット則を満たすように結合を形成する
- 半導体、または伝導度の低い伝導体
- 主に反磁性または常磁性体
- 金属光沢を示すが脆い
一方で、陰イオンが孤立していてもZintl相と呼ばれる場合があり、厳密なルールという訳ではありません.典型元素のみからなる物質がZintl相とされますが、遷移金属を含んだ系に拡張されるケースもあります.
Zintl相と機能
Zintl相の定義を取り上げましたが、例が一つだけでは心もとないかもしれません.以下では、もう少し具体的な例と機能について見ていきます.
NaSi
電気的に陽性な元素であると少し陰性な
からなる化合物です.
がカチオンになった場合、
1つあたりが受け取る電子数は1つです.このとき、
は15族元素と同じ電子配置となります.15族元素と言えば、アンモニア(
)の構造を思い出せば分かるように、3つの結合電子と1セットの孤立電子対を持ちます.
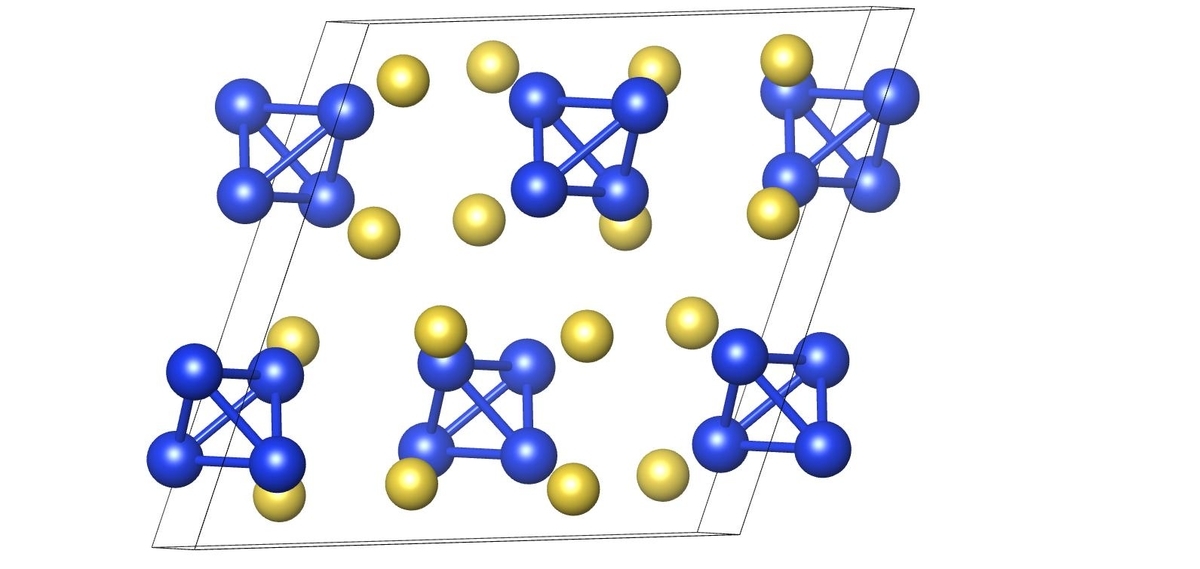
実際、中における
はそれぞれ3つの
と結合を組んでおり、4つの
からなる正四面体型のクラスターを形成します.これは、単体のリン(15族元素)で見られる四面体とよく似ています.
は、不燃性・空気安定性の高い粉末で、水と瞬時に反応して純粋な水素が発生します.
は、純粋な
よりも単位重量あたりの水素発生量が多いばかりか、安全性・保存性に優れるため、燃料電池用の水素発生源として注目されています.
また、を熱分解することでカゴ型のクラスレート
や
が生成します.
CaSb2
では、電気的に陽性な
から
に電子が受け渡されます.
は2価のカチオンであるため、
1つあたり1つの電子を受け取り、16族元素と同じ電子配置となります.
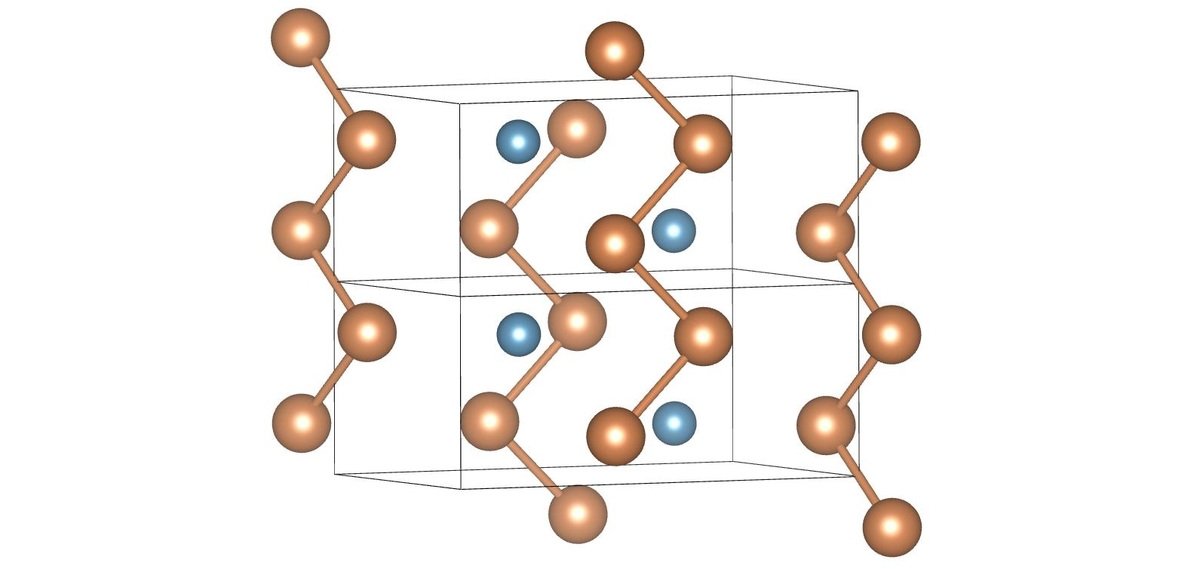
16族元素は、水の構造を思い出せば分かる通り、2つの結合電子と2セットの孤立電子対を持ちます.の結晶構造では、
のジグザグな一次元鎖が見られます.
1つあたり2つの結合を形成しており、オクテット則を満たします.
なぜ真っ直ぐではなくジグザグであるのかと言えば、水が折れ線状であることと同様、孤立電子対が存在することを反映しています.
の物性測定は長らくされていませんでしたが、最近では、トポロジカル半金属の一種であることおよび低温で超伝導を示すことが報告されています.
MgB2
の
は13族元素であり、
から電子を提供されることで14族元素と同じ電子配置となります.
と同じ電子配置ですがアニオンのネットワークは異なります.
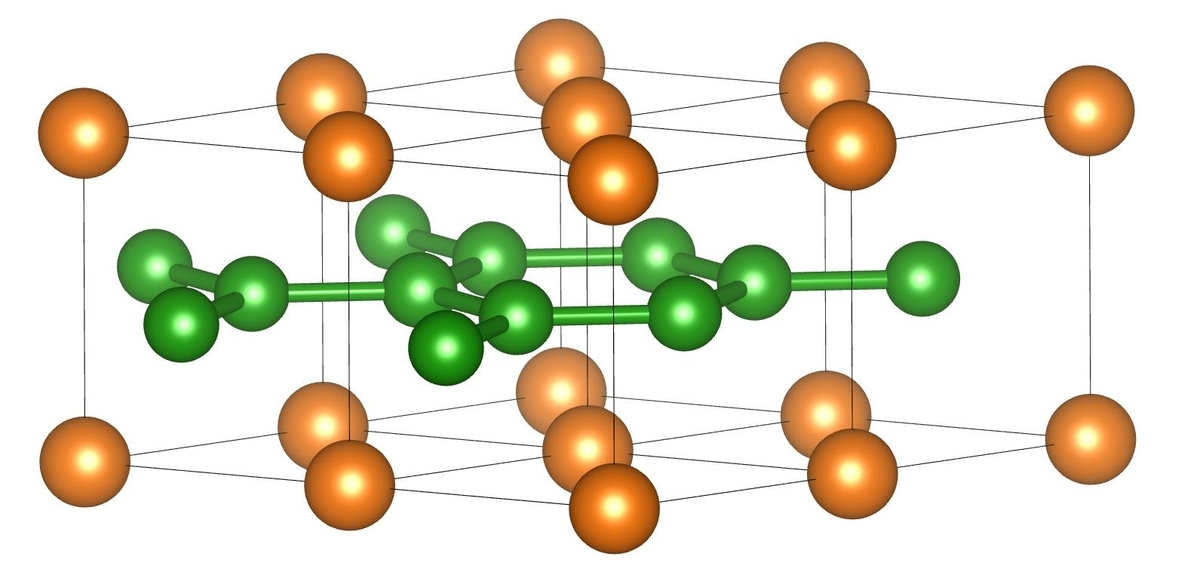
代わりに、グラファイトのように層状のハニカム構造が見られます.は、
型構造と呼ばれる結晶構造グループの一因ですが、
はオクテット則を満たしません.オクテット則は普遍的なように見えて、必ずしも成り立っているとは限らないのです.
は高い転移温度を持つ超伝導体としてあまりにも有名です.
型構造を持つ物質には他にも珍しい物性を示す物が多く、トポロジカル半金属
やスキルミオンを示す
などが挙げられます.こうして見ると、オクテット則が成り立っていない物質も多いですね.
まとめ
Zintl相は日本ではそれほど知名度が高くありませんが、多くの物質が属する非常に大きな物質グループです.それゆえ、これまでに多種多様な結晶構造、多彩な物性が知られています.特に、重元素から構成され、半導体的な伝導性を持つという特徴は熱電材料にとって都合が良く、それゆえ熱電変換に資する材料としての研究が近年非常に多くなっています.
こうした結晶構造や電子数に基づいた分類は、物理畑の人から顧みられることは少ないですが、類似の物質を探索・予言する上で大きな威力を発揮します.多くのポリアニオンネットワークはZintl-Klemm則で説明可能ですが、このルールに従わない物質も存在します.新たに超原子価結合などの理論が生み出され、全ての結合様式を説明できる理論の完成に向けた努力が続けられています.
参考文献
高圧力の科学と技術 2014 年 24 巻 3 号 p. 195-203
日本結晶学会誌 2005 年 47 巻 5 号 p. 323-333
Fässler, Thomas F., ed. "Zintl phases: principles and recent developments." (2011).
Silicide-Based Hydrogen Generation for Back-Up Power and Portable Fuel Cells (Wayback Machine)
Materials Today: Proceedings, 2018, 5.2: 3563-3570.
Journal of the Physical Society of Japan 88.4 (2019): 044711.
Physical Review Materials 4.4 (2020): 041801.
結晶構造の描画にはVESTAを使用.K. Momma and F. Izumi, "VESTA 3 for three-dimensional visualization of crystal, volumetric and morphology data," J. Appl. Crystallogr., 44, 1272-1276 (2011).